MINISTERUL SĂNĂTĂȚII AGENȚIA NATIONALĂ A MEDICAMENTULUI SI A DISPOZITIVELOR MEDICALE Str. Av. Sănătescu nr. 48, sector 1, Bucureşti Tel:
|
|
|
- Marius Preda
- 4 ani în urmă
- Vzualizari:
Transcriere
1 RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: BRENTUXIMAB VEDOTIN INDICAŢIA: LIMFOM HODGKIN (LH) CD30+ STADIUL IV, NETRATAT ANTERIOR, ÎN ASOCIERE CU DOXORUBICINĂ, VINBLASTINĂ ȘI DACARBAZINĂ (AVD) Data depunerii dosarului Număr dosar 174 PUNCTAJ: 80
2 1. DATE GENERALE 1.1. DCI: Brentuximab Vedotin 1.2. DC: Adcetris 50 mg pulbere pentru concentrat pentru soluţie perfuzabilă 1.3 Cod ATC: L01XC Data eliberării APP: Deținătorul APP: Takeda Pharma A/S, Danemarca 1.6. Tip DCI: orfană 1.7. Forma farmaceutică, concentrația, calea de administrare, mărimea ambalajului Forma farmaceutică pulbere concentrat pentru soluţie perfuzabilă Concentraţie 50 mg Calea de administrare intravenoasă Mărimea ambalajului cutie cu 1 flacon de 50mg pulbere concentrat pentru soluţie perfuzabilă 1.8. Preț conform Ordinului ministrului sănătății nr din 21 noiembrie 2018 Preţul cu amănuntul pe ambalaj Preţul cu amănuntul pe unitatea terapeutică 14, lei 14, lei 1.9. Indicația terapeutică și doza de administrare conform RCP Adcetris Indicaţie terapeutică ADCETRIS este indicat pentru pacienții adulți cu limfom Hodgkin (LH) CD30+ stadiul IV, netratat anterior, în asociere cu doxorubicină, vinblastină și dacarbazină (AVD) Doza recomandată Doza recomandată în asociere cu chimioterapie (doxorubicină [A], vinblastină [V] și dacarbazină [D] [AVD]) este de 1,2 mg/kg administrată prin perfuzie intravenoasă într-un interval de 30 minute în zilele 1 și 15 ale fiecărui ciclu de 28 zile, timp de 6 cicluri Durata medie a tratamentului conform RCP Tratamentul trebuie continuat până la progresia bolii sau apariția toxicității inacceptabile. Numărul mediu de cicluri administrate este de 6 cicluri. Informații suplimentare din RCP Adcetris: Grupe speciale de pacienți: Insuficiență renală: Pacienții cu insuficiență renală trebuie monitorizați îndeaproape pentru depistarea evenimentelor adverse. Nu există experiență din studii clinice cu utilizarea ADCETRIS în asociere cu chimioterapie la pacienți cu insuficiență renală la care valoarea creatininei serice este 2,0 mg/dl și/sau clearance-ul creatininei sau clearance-ul calculat al creatininei este 40 ml/minut. Utilizarea ADCETRIS în asociere cu chimioterapie trebuie evitată la pacienții cu insuficiență renală severă. Insuficiență hepatică: Pacienții cu insuficiență hepatică trebuie monitorizați îndeaproape pentru depistarea evenimentelor adverse. Doza inițială recomandată la pacienții cu insuficiență hepatică ușoară este 0,9 mg/kg administrată prin perfuzie intravenoasă într-un interval de 30 minute, o dată la 3 săptămâni. Nu există experiență din studii clinice cu utilizarea ADCETRIS în asociere cu chimioterapie la pacienți cu insuficiență hepatică la care valoarea
3 bilirubinei totale este > 1,5 ori limita superioară a valorilor normale (LSVN) (exceptând cazul în care este cauzată de sindromul Gilbert) sau valoarea aspartataminotransferazei (AST) sau a alaninaminotransferazei (ALT) este > 3 ori LSVN sau > 5 ori 6 LSVN dacă creșterea poate fi atribuită în mod justificat prezenței LH la nivel hepatic. Utilizarea ADCETRIS în asociere cu chimioterapie trebuie evitată la pacienții cu insuficiență hepatică moderată și severă. Vârstnici: Pe baza analizelor de farmacocinetică populațională și a profilului de siguranță la pacienţii vârstnici, care sunt în concordanță cu cele observate la pacienții adulți, recomandările de doze pentru pacienții cu vârsta de 65 de ani şi peste sunt aceleași cu cele pentru adulți. Copii şi adolescenţi: Siguranţa şi eficacitatea la copii cu vârsta sub 18 ani nu au fost încă stabilite. 2. GENERALITĂȚI PRIVIND PRIVIND LIMFOMUL HODGKIN Limfomul Hodgkin (anterior, boala Hodgkin) este un limfom potențial curabil cu histologie, comportament biologic și caracteristici clinice distincte. Boala este definită în ceea ce privește aspectul microscopic (histologic) și expresia markerilor de suprafață celulară (imunofenotip). Pentru a diagnostica limfomul Hodgkin o evaluare histologică este întotdeauna necesară și o biopsie excizională a ganglionilor limfatici este recomandată pentru acest scop. Diverse studii imagistice sunt utilizate pentru stadializarea bolii pacientului. IN SUA, NCI/SEER raporteaza ca rata incidenței (cazuri noi) limfomului Hodgkin a fost în scădere, în medie, cu 1,2 % în fiecare an, în ultimii 10 de ani. Începând cu , incidența ajustată în funcție de vârstă este de 2, 6 cazuri la de locuitori. Rata de deces a fost în scădere, în medie, cu 2,6% în fiecare an in perioada Incidența la nivel mondial a limfomului Hodgkin a rămas relativ stabila. În Europa și în alte țări dezvoltate, incidența merge paralel cu cea din SUA. Date din Regatul Unit din 2013 arată o rată a incidenței brută de 3, 5 cazuri la de bărbați și 2,6 cazuri la de femei. In Romania incidenta ajustata in functie de varsta estimata pentru anul 2012 este de 1,4 la de locuitori iar mortalitatea ajustata in functie de varsta este de 0,4 la de locuitori. Incidenta limfomului Hodgkin in Statele Unite variaza in functie de rasa si sex. In general, incidenta este mai mare la bărbați decât la femei. Predilecția de sex este cea mai pronunțată la copii, cu 85% din cazuri care afectează băieții. Cea mai mică incidență se gaseste la asiatici si populatia din Isulele din Pacific. Incidența limfomului Hodgkin variază în funcție de vârstă, cu o distribuție bimodală clara care este consecventă în majoritatea țărilor și studiilor. Varful inițial este la adulții tineri (15-34 ani) si adultii in varsta (> 55 ani). Există, de asemenea, o diferență de subtip în funcție de vârstă, cu tinerii adulți care au limfom Hodgkin scleroza nodulara (LHSN) si adulti in varsta care tind sa aiba limfom Hodgkin, celularitate mixta (LHCM). Clasificarea limfomului Hodgkin (WHO şi REAL) I. Boala Hodgkin nodulară predominent limfocitară II. Boala Hodgkin clasică: 1. Boala Hodgkin cu predominentă limfocitară 2. Boala Hodgkin scleroza nodulară 3. Boala Hodgkin cu celularitate mixtă 4. Boala Hodgkin cu depleţie limfocitară
4 Stadializarea este efectuată conform sistemului Ann Arbor şi ţine cont de factorii de risc enumeraţi în Tabelul 1. După finalizarea stadializării, pacienţii sunt grupaţi în trei categorii, iar tratamentul este ales în funcţie de acestea (stadiile limitat, intermediar sau avansat) [II III, A]. Diagnosticul este stabilit pe baza examenului histopatologic al ganglionului biopsiat prin biopsie excizionala. Biopsia tru-cut poate fi adecvata pentru diagnostic, dar se recomanda biopsie ganglionara excizionala. Cu toate ca aspiratia cu ac fin (FNA) este utilizata pe scară largă în diagnosticul tumorilor maligne, rolul său în diagnosticul limfomului este inca controversata si un diagnostic de limfom nu poate fi exclus printr-o biopsie FNA negativa. Biopsia FNA trebuie evitată și este considerata a fi adecvata, împreună cu IHC numai atunci cand este diagnostica de LH, de către un expert hematopatologist sau citopathologist. Aspiraţia cu ac fin este utilizată la pacienţii cu Boală Hodgkin cunoscută, pentru a evalua o recidivă sau boală reziduală. Se recomandă evaluarea IHC. Celulele Reed-Sternberg de LHC exprima CD15 și CD30 în majoritatea pacienților și sunt, de obicei negative pentru CD3 și CD45. Celulele L& H din LHNPL sunt de obicei CD45 + și CD20 +, nu exprima CD3 sau CD15 și rareori exprima CD30. În plus, celulele L& H din LHNPL exprimă antigen epithelial de membrană, care de obicei care nu este prezent în LHC. 3. PREVEDERILE AGENȚIEI EUROPENE A MEDICAMENTULUI REFERITOARE LA STATUTUL DE MEDICAMENT ORFAN Statutul de medicament orfan pentru brentuximab vedotin a fost re-acordat companiei Takeda Global Research and Development Center Ltd. din Regatul Unit de către Comisia Europeană la data de 6 Februarie 2019 si pentru tratamentul limfomului Hodgkin (LH) CD30+ stadiul IV, netratat anterior, în asociere cu doxorubicină, vinblastină și dacarbazină (AVD). În data de , Comitetul pentru produse medicamentoase orfane din cadrul Agenției Europene a Medicamentului a decis acordarea statutului de medicament orfan pentru brentuximab vedotin în indicația: tratamentul limfomului Hodgkin. Raportul, datat 13 noiembrie 2013, publicat pe site-ul Agenției Europene a Medicamentului, cuprinde rezumatul evaluării inițiale, din 2009, a brentuximabului vedotin, de către Comitetul pentru produse medicamentoase orfane. Concluziile raportului inițial au fost următoarele: limfomul Hodgkin este o boală severă, a cărei diagnosticare și tratare precoce, poate duce la vindecare; însă vindecarea prin aplicarea tratamentelor standard, nu este o regulă, pentru toți pacienții.
5 o persoană din de locuitori din Uniunea Europeană este diagnosticată cu limfom Hodgkin. În anul 2012, a fost reanalizat statutul de medicament orfan al brentuximab vedotin. Raportul, datat 27 noiembrie 2012, publicat pe site-ul Agenției Europene a Medicamentului cuprinde această reevaluare. Concluziile celui de-al doilea raport de evaluare, au fost următoarele: limfomul Hodgkin este o boală severă, cu un prognostic slab, în ceea ce privește supraviețuirea pacienților refractari la tratamentul administrat sau care prezintă recăderi după tratamentul standard aplicat 5 persoane din de locuitori din Uniunea Europeană sunt diagnosticate cu limfom Hodgkin. In anul 2019, a fost reanalizat statutul de medicament orfan al brentuximab vedotin. Raportul, datat in 6 Februarie 2019 publicat pe site-ul Agenției Europene a Medicamentului cuprinde această reevaluare. Conform acestui raport, comitetul pentru produse medicamentoase orfane a decis că brentuximab vedotin in noua indicație care face obiectul acestei evaluari, se încadrează în statutul de orfan menționat anterior. Brentuximab vedotin este un complex anticorp-medicament (ADC), care oferă un agent antineoplazic ce determină moartea celulelor apoptotice în mod selectiv în celulele tumorale care exprimă CD30-. Legarea complexului ADC de CD30 de pe suprafaţa celulelor iniţiază internalizarea complexului ADC-CD30, care apoi circulă către compartimentul lizozomal. În interiorul celulei, o specie activă definită unică, MMAE, este eliberată prin scindare proteolitică. Legarea MMAE de tubulină dislocă reţeaua microtuburilor din interiorul celulei, induce oprirea ciclului celular şi are ca rezultat moartea apoptotică a celulelor tumorale care exprimă CD30. LH clasic, LACMs și subtipurile LCCT (inclusiv MF și LACMpc) exprimă CD30 ca antigen pe suprafaţa celulelor sale maligne. Această exprimare este independentă de stadiul bolii, linia terapeutică sau starea transplantului. Aceste caracteristici fac din CD30 o ţintă pentru intervenţia terapeutică. Datorită mecanismului de acţiune asupra ţintei CD30, brentuximab vedotin este capabil să depăşească chimio-rezistenţa CD30 care este în mod constant exprimat la pacienţi care sunt refractari la chimioterapia cu medicamente multiple, indiferent de statusul înainte de transplant. Mecanismul de acţiune ţintit asupra CD30 a brentuximab vedotin, exprimarea în mod constant a CD30 în LH clasic, LACMs și LCCT CD30+ şi spectrul terapeutic şi evidenţa clinică în bolile maligne cu CD30 pozitiv după multiple linii terapeutice, oferă o raţiune biologică pentru utilizarea sa la pacienţi cu LH clasic, LACMs recidivat şi refractar cu sau fără TCSA și LCCT CD30+ prealabil după cel puțin 1 tratament sistemic anterior. Pentru justificarea existenței beneficiului semnificativ adus de terapia cu brentuximab vedotin au fost prezentate rezultatele studiului clinic de fază III, ECHELON-1: studiu multicentric randomizat, în regim deschis, cu 2 grupuri de tratament, efectuat la 1334 pacienți cu LH avansat netratat anterior în asociere cu chimioterapie (doxorubicină [A], vinblastină [V] și dacarbazină [D] [AVD]). Toți pacienții aveau boală cu expresie CD30 confirmată histologic. 62% dintre pacienți prezentau implicare extranodală. Dintre cei 1334 pacienți, 664 pacienți au fost randomizați la grupul de tratament cu ADCETRIS + AVD, iar 670 pacienți au fost randomizați la grupul de tratament cu ABVD (doxorubicină [A], bleomicină [B], vinblastină [V] și dacarbazină [D] [AVD]) și stratificați în funcție de numărul de factori de risc conform Proiectului Internațional privind Factorii de Prognostic (International Pronostic Factor Project IPFP) și de regiune. Pacienții au fost tratați în zilele 1 și 15 ale fiecărui ciclu de 28 zile cu ADCETRIS 1,2 mg/kg administrat prin perfuzie intravenoasă într un interval de 30 minute + doxorubicină 25 mg/m2, vinblastină 6 mg/m2 și dacarbazină 375 mg/m2. Numărul mediu de cicluri administrate a fost 6 (interval: 1 6 cicluri). Tabelul 4 prezintă un rezumat al caracteristicilor inițiale ale pacienților și ale bolii. Nu au existat diferențe relevante între caracteristicile pacienților și ale bolii dintre cele două brațe.
6 Tabelul 4: Rezumatul caracteristicilor pacienților și ale bolii în studiul de fază 3 cu LH netratat anterior Caracteristicile pacienților ADCETRIS + AVD n = 664 ABVD n = 670 Media de vârstă (interval) 35 ani (18-82) 37 ani (18-83) Pacienți 65 ani, n (%) 60 (9) 62 (9) Sex, n (%) 378M (57) 286F (43) 398M (59) 272F (41) Indice ECOG, n (%) (57) 378 (57) (39) 263 (39) 2 28 (4) 27 (4) Absent 0 2 Caracteristicile bolii Timpul mediu de la diagnosticul de LH până la prima doză (interval) Stadiul bolii a la diagnosticul inițial de LH, n (%) 0,92 luni (0,1-21,4) 0,89 luni (0,0-81,4) III 237 (36) 246 (37) IV 425 (64) 421 (63) Nu este cazul 1 (< 1) 1 (< 1) Absent 0 2 (< 1) Implicare extranodală la momentul diagnosticului, n (%) Factori de risc IPFP b, n (%) 411 (62) 416 (62) (21) 141 (21) (53) 351 (52) (25) 178 (27) Implicarea măduvei osoase la momentul 147(22) 151 (23) diagnosticului sau al includerii în studiu, n (%) Simptome B a, n (%) 400 (60) 381 (57) a Conform stadializării Ann Arbor b IPFP = Proiectul Internațional privind Factorii de Prognostic Criteriul final principal de evaluare în cadrul Studiului C25003 l-a constituit SFP modificată (SFPm) conform Independent Review Facility (IRF), definită ca timpul de la randomizare până la evoluția bolii, deces sau dovezi de răspuns non-complet (Rnon-C) după finalizarea tratamentului de primă linie conform IRF, urmat de tratament antineoplazic. Momentul atribuit evenimentului modificat l-a constituit data primei scanări PET după finalizarea tratamentului de primă linie care a demonstrat absența răspunsului complet (RC), definit printr-un scor Deauville 3. SFP modificată medie conform evaluării IRF nu a fost atinsă în niciunul dintre grupurile de tratament. Rezultatele la populația cu intenție de tratament (ITT) au arătat o îmbunătățire semnificativă statistic a SFP modificată pentru ADCETRIS + AVD, cu un raport de risc stratificat de 0,770 (IÎ 95%, 0,603; 0,983, p = 0,035), ceea ce indică o reducere cu 23% a riscului de evenimente aferente SFP modificată pentru ADCETRIS + AVD comparativ cu ABVD.
7 O analiză pre-specificată, pe subgrupe, a SFPm în funcție de stadiul bolii a arătat că pacienții cu boală în Stadiul IV au prezentat un efect mai amplu comparativ cu populația ITT, cu un raport de risc nestratificat de 0,71 (IÎ 95%, 0,53; 0,96), compatibil cu o reducere cu 29% a riscului de evenimente aferente SFP modificată pentru ADCETRIS + AVD comparativ cu ABVD. În cadrul populației ITT, 846 pacienți (64%) aveau boală în Stadiul IV. Tabelul 5 prezintă rezultatele de eficacitate pentru SFP modificată și supraviețuirea globală (SG) la populația ITT și la pacienții cu boală în Stadiul IV. Tabelul 5: Rezultate de eficacitate pentru pacienți cu LH netratat anterior, tratați cu 1,2 mg/kg ADCETRIS + AVD în zilele 1 și 15 ale unui ciclu de 28 zile (ITT și Stadiul IV) Număr de evenimente (%) Populație cu intenție de tratament (ITT) ADCETRIS + AVD n = 664 ABVD n = (18) 146 (22) Raport de risc stratificat și valoarea p Pacienți cu boală în Stadiul IV ADCETRIS + AVD n = 425 ABVD n = (18) 102 (24) Raport de risc nestratificat și valoarea p SFPm estimată a conform IRF la 2 ani (%) 82,1 (IÎ 95% [78,8; 85,0]) 77,2 (IÎ 95% [73,7; 80,4]) 0,77 (IÎ 95% [0,60; 0,98]) valoarea p=0,035 82,0 (IÎ 95% [77,8; 85,5]) 75,3 (IÎ 95% [70,6; 79,3]) 0,71 (IÎ 95% [0,53; 0,96]) valoarea p=0,023 Supraviețuire globală b Număr de decese (%) 28 (4) 39 (6) 0,73 (IÎ 95% [0,45; 1,18]) valoarea p=0, (3) 26 (6) 0,51 (IÎ 95% [0,27; 0,97]) valoarea p=0,037 a La momentul analizei, timpul mediu de urmărire pentru SFP modificată pentru ambele grupuri de tratament a fost 24,6 luni b Date provenite dintr-o analiză SG intermediară Figura 1: Supraviețuirea fără progresia bolii, modificată, conform IRF la populația ITT (ADCETRIS + AVD comparativ cu ABVD)
8 Figura 2: Supraviețuirea fără progresia bolii, modificată, conform IRF la pacienții cu boală în Stadiul IV (ADCETRIS + AVD comparativ cu ABVD) Alte criterii finale secundare de evaluare a eficacității, incluzând rata RC și RRO la finalul schemei de randomizare, rata RC la finalul tratamentului de primă linie și rata negativității PET la finalul Ciclului 2, durata răspunsului (DR), durata remisiunii complete (DRC), supraviețuirea fără boală (SFB) și supraviețuirea fără evenimente (SFE), toate acestea au prezentat tendințe în favoarea ADCETRIS + AVD atât la populația ITT, cât și la populația cu boală în Stadiul IV. Au fost efectuate analize pre-specificate ale SFP conform IRF, pe subgrupe, la populația ITT, iar acestea au inclus vârsta, regiunea, stadiul cancerului la momentul inițial, locurile extranodale la momentul inițial, numărul de factori de risc IPFP, simptomele B la momentul inițial, evaluarea PET în Ciclul 2, scorul Deauville PET în Ciclul 2 și administrarea medicamentelor alternative de primă linie (AFM). Analizele au arătat o tendință consecventă către beneficiul pacienților cărora li s a administrat ADCETRIS + AVD comparativ cu pacienții cărora li s a administrat ABVD în majoritatea subgrupurilor. Eficacitatea în grupurile de pacienți vârstnici (pacienți 60 ani [n = 186] [RR = 1,00, IÎ 95% (0,58; 1,72)] și 65 ani [n = 122] [RR = 1,01, IÎ 95% (0,53; 1,94)]) și la pacienții fără locuri extranodale (n = 445) (RR = 1,04, IÎ 95% [0,67; 1,62]) nu au arătat diferențe semnificative clinice între cele două grupuri de tratament. Au fost efectuate analize post hoc pe subgrupe ale SFP modificată conform IRF pentru pacienții cu boală în stadiul IV, iar acestea au inclus vârsta, regiunea, locurile extranodale la momentul inițial, numărul de factori de risc IPFP, simptomele B la momentul inițial, indicele ECOG la momentul inițial și sexul. Analizele au arătat o tendință consecventă către beneficiul pacienților cărora li s a administrat ADCETRIS + AVD comparativ cu pacienții cărora li s a administrat ABVD în majoritatea subgrupurilor. Pacienții cu boală în stadiul IV pentru care s a raportat boală extranodală ([n = 722] [HR = 0,69, IÎ 95% (0,50; 0,94)]) au prezentat un beneficiu SFPm (per IRF). Pacienții cu boală în stadiul IV pentru care nu s a raportat boală extranodală, niciun beneficiu nu a fost demonstrat la momentul analizei ([n = 85] [RR = 1,49, IÎ 95% (0,51; 4,31)]). Semnificația acestei constatări la pacienții cu LH în stadiul IV fără boală extranodală nu este stabilită din cauza numărului mic de pacienți și a ratei scăzute de evenimente (14 evenimente). Eficacitatea la pacienții vârstnici cu boală în Stadiul IV din grupul cu A + AVD (pacienți 60 ani [n = 118] [RR = 0,80, IÎ 95% (0,42; 1,53)] și 65 ani [n = 78] [RR = 0,78, IÎ 95% (0,36; 1,67)]) a arătat un beneficiu îmbunătățit comparativ cu pacienții vârstnici din cadrul populației ITT.
9 În cadrul populației ITT, chimioterapia ulterioară de urgență (n = 66) și chimioterapia în doză crescută și transplantul (n = 36) au fost utilizate la un procent de pacienți cu 33% mai mic în cadrul populației ITT tratate cu ADCETRIS + AVD comparativ cu pacienții tratați cu ABVD (n = 99, respectiv n = 54). La populația cu boală în Stadiul IV, chimioterapia ulterioară de urgență (n = 45) a fost utilizată la un procent de pacienți cu 35% mai mic în grupul tratat cu ADCETRIS + AVD comparativ cu pacienții tratați cu ABVD (n = 69), iar chimioterapia în doză crescută și transplantul (n = 29) au fost utilizate la un procent de pacienți cu 22% mai mic în grupul tratat cu ADCETRIS + AVD comparativ cu pacienții tratați cu ABVD (n = 37). Chestionarul cu 30 itemi al Organizației Europene pentru Cercetare și Tratament privind Calitatea Vieții cu Cancer (EORTC QLQ C30) nu a arătat diferențe semnificative clinic între cele două grupuri de tratament, atât la populația ITT, cât și la populația cu boală în Stadiul IV. În urma reevaluării, Comitetul pentru produse medicamentoase orfane, din cadrul Agenției Europene a Medicamentului a concluzionat că Adcetris rămâne încadrat ca medicament orfan. 4. RECOMANDĂRILE GHIDURILOR INTERNAȚIONALE PRIVIND TRATAMENTUL LIMFOMULUI HODGKIN (LH) CD30+ STADIUL IV, NETRATAT ANTERIOR, ÎN ASOCIERE CU DOXORUBICINĂ, VINBLASTINĂ ȘI DACARBAZINĂ (AVD) 4.1. GHIDUL EUROPEAN DE ONCOLOGIE Dupa diagnosticul de LH, regimurile de chimioterapie si radioterapie sunt recomandate, in functie de stadiul bolii. Dupa Ghidul ESMO (Eichenauer et al, 2018), urmatorul algoritm terapuetic poate fi folosit: HL, Hodgkin s lymphoma; RT, radiotherapy; ABVD, adriamycin, bleomycin, vinblastine, dacarbazine; BEACOPPesc, bleomycin, etoposide, adriamycin, cyclophosphamide, vincristine, procarbazine, prednisone escalated dose regimen; ISRT, involved-site radiotherapy; PET, positron emission tomography; NLPHL, nodular lymphocyte-predominant Hodgkin s lymphoma; IFRT, involved field RT
10 În prezent, standardul de îngrijire în LH în stadii limitate este reprezentat de două pana la 4 cicluri de adriamicină/ bleomicină/vinblastină/dacarbazină (ABVD) urmate sau nu de radioterapie pe câmpuri limitate. Această abordare are drept rezultat rate de creștere de 3 până la 5 ani fără progresia bolii și rate de supravietuire generala care depășesc 90%, respectiv 95% la pacienții cu boală favorabilă și 85%, respectiv 90% la pacienții cu boală nefavorabilă. LH în stadiul avansat este tratat de obicei cu 6-8 cicluri de ABVD. Radioterapia este rezervată pentru pacienţii cu mase tumorale reziduale mari după chimioterapie. Rata de supravietuire fara progresie a fost intre 61% si 67% iar supravietuirea generala la 5 ani intre 73% si 85%, in multiple studii care au inrolat pacienti LH stadiul III/IV. Pacienţii în vârstă de până la 60 de ani, care sunt eligibili pentru un tratament mai intens, BEACOPP escaladat BEACOPP (bleomycin,etoposide, doxorubicin, cyclophosphamide, vincristine, procarbazine, and prednisone) poate fi luata in considerare. Totusi BEACOPP escaladat nu ar trebui administrat pacientilor > 60 ani, deoarece cresterea mortalitatii legata de tratament a fost observata la aceasta categorie de varsta. Un studiu recent, randomizat a aratat o imbunatatire a mpfs dupa 6 cicluri de brentuximab vedotin in combinatie cu AVD (A-AVD) comparativ cu chimioterapia standard ABVD. La majoritatea pacienţilor cu LH refractar sau recidivat, tratamentul de elecţie poate fi considerat chimioterapia în doze mari urmată de transplant autolog de celule stem (TACS). Administrarea de brentuximab vedotin reprezinta o optiune la pacientii care au recazut dupa TCSA sau au un risc crescut de recadere dupa ASCT GHIDUL AMERICAN DE ONCOLOGIE În versiunea 3 a ghidului clinic publicat in anul 2018 de catre Societatea Americana de Oncologie (NCCN) pentru limfomul Hodgkin stadiul III-IV sunt propuse optiunile terapeutice din tabelul de mai jos, Brentuximab vedotin (BV) + AVD (6 cicluri) fiind una dintre opțiuni:
11 5. RAMBURSAREA MEDICAMENTULUI ÎN STATELE MEMBRE ALE UNIUNII EUROPENE Medicamentul brentuximab vedotin este rambursat în 23 de state membre ale Uniunii Europene: Austria, Belgia, Bulgaria, Croatia, Danemarca, Estonia, Finlanda, Franța, Germania, Grecia, Ungaria, Irlanda, Italia, Lituania, Luxemburg, Marea Britanie, Olanda, Polonia, Portugalia, Slovacia, Slovenia, Spania și Suedia. 6. EVALUĂRI INTERNAȚIONALE Evaluările internationale din Franța, Marea Britanie și Germania pentru DCI brentuximab vedotin cu indicația limfom Hodgkin (LH) CD30+ stadiul IV, netratat anterior, în asociere cu doxorubicină, vinblastină și dacarbazină (AVD) sunt listate în tabelul următor: Tabel 3: Concluziile rapoartelor de evaluare internatională a medicamentului brentuximab vedotin cu indicația:,,limfom Hodgkin (LH) CD30+ stadiul IV, netratat anterior, în asociere cu doxorubicină, vinblastină și dacarbazină (AVD)" Autoritatea de evaluare a tehnologiilor medicale Data Referinta Concluzii raport HAS Nu a fost publicat raportul - NICE Nu a fost publicat raportul - SMC Nu a fost publicat raportul - IQWIG Nu a fost publicat raportul - G-BA Nu a fost publicat raportul - 7. PUNCTAJ Criterii de evaluare Nr. puncte Tratamentul, prevenirea sau diagnosticarea unor afecțiuni care nu afectează mai mult de 5 din de persoane din UE sau care pun în pericol viața, sunt cronic debilitante sau reprezintă afecțiuni grave și cronice ale organismului. În plus pentru 55 aceste boli nu există nici o metodă satisfăcătoare de diagnosticare, prevenire sau tratament autorizată în UE sau, dacă această metodă există, medicamentul aduce un beneficiu terapeutic semnificativ celor care suferă de această acțiune. Statutul de compensare al medicamentului cu DCI brentuximab vedotin în statele 25 membre ale UE 23 state Total Punctaj 80
12 8. CONCLUZII Conform O.M.S. 387/2015 care modifică și completează O.M.S. 861/2014 privind aprobarea criteriilor și metodologiei de evaluare a tehnologiilor medicale, medicamentul cu DCI brentuximab vedotin întrunește, pentru indicația,,limfom Hodgkin (LH) CD30+ stadiul IV, netratat anterior, în asociere cu doxorubicină, vinblastină și dacarbazină (AVD) punctajul de admitere necondiționată în Lista care cuprinde denumirile comune internaționale corespunzătoare medicamentelor de care beneficiază asigurații, cu sau fără contribuție personală, pe bază de prescripție medicală, în sistemul de asigurări sociale de sănătate. 9. RECOMANDĂRI Recomandăm elaborarea protocolului terapeutic pentru medicamentul cu DCI brentuximab vedotin având indicația,,limfom Hodgkin (LH) CD30+ stadiul IV, netratat anterior, în asociere cu doxorubicină, vinblastină și dacarbazină (AVD). Realizat şi întocmit Dr. Alina Malaescu Şef DETM Dr. Farm. Pr.Felicia Ciulu Costinescu
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE
 RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: BRENTUXIMAB VEDOTIN INDICAŢIA: LIMFOM HODGKIN CD30+ RECIDIVAT SAU REFRACTAR: 1. DUPĂ TRANSPLANT DE CELULE STEM AUTOLOGE (TCSA) 2. DUPĂ CEL PUŢIN DOUĂ TRATAMENTE
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: BRENTUXIMAB VEDOTIN INDICAŢIA: LIMFOM HODGKIN CD30+ RECIDIVAT SAU REFRACTAR: 1. DUPĂ TRANSPLANT DE CELULE STEM AUTOLOGE (TCSA) 2. DUPĂ CEL PUŢIN DOUĂ TRATAMENTE
RAPORT
 RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE NIVOLUMABUM INDICAȚIA: MONOTERAPIE PENTRU TRATAMENTUL CANCERULUI SCUAMOS DE CAP SI GAT LA ADULTI LA CARE BOALA PROGRESEAZA IN TIMPUL SAU DUPA TERAPIE DE BAZA
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE NIVOLUMABUM INDICAȚIA: MONOTERAPIE PENTRU TRATAMENTUL CANCERULUI SCUAMOS DE CAP SI GAT LA ADULTI LA CARE BOALA PROGRESEAZA IN TIMPUL SAU DUPA TERAPIE DE BAZA
MINISTERUL SĂNĂTĂȚII AGENȚIA NAȚIONALĂ A MEDICAMENTULUI ȘI A DISPOZITIVELOR MEDICALE Departamentul de Evaluare a Tehnologiilor Medicale Str. Aviator S
 RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: RIOCIGUAT INDICAȚII: HIPERTENSIUNE ARTERIALĂ PULMONARĂ CRONICĂ HIPOEMBOLICĂ (HAPCTE) HIPERTENSIUNE ARTERIALĂ PULMONARĂ (HAP) Data depunerii dosarului 08.04.2015
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: RIOCIGUAT INDICAȚII: HIPERTENSIUNE ARTERIALĂ PULMONARĂ CRONICĂ HIPOEMBOLICĂ (HAPCTE) HIPERTENSIUNE ARTERIALĂ PULMONARĂ (HAP) Data depunerii dosarului 08.04.2015
MINISTERUL SĂNĂTĂȚII AGENȚIA NAȚIONALĂ A MEDICAMENTULUI ȘI A DISPOZITIVELOR MEDICALE Departamentul de Evaluare a Tehnologiilor Medicale Str. Aviator S
 RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE BENDAMUSTINUM INDICAȚIA: LIMFOM nonhodkin Data de depunere dosar 18.08.2014 Numar dosar 3143 PUNCTAJ: 65 1 1. DATE GENERALE 1.1. DCI: BENDAMUSTINUM 1.2. DC:
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE BENDAMUSTINUM INDICAȚIA: LIMFOM nonhodkin Data de depunere dosar 18.08.2014 Numar dosar 3143 PUNCTAJ: 65 1 1. DATE GENERALE 1.1. DCI: BENDAMUSTINUM 1.2. DC:
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE
 RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DABRAFENIBUM INDICAȚIA: MELANOM INOPERABIL SAU METASTATIC POZITIV LA MUTATIA BRAF V600 Data de depunere dosar 11.08.2014 Numar dosar 3035 PUNCTAJ: 65 1. DATE
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DABRAFENIBUM INDICAȚIA: MELANOM INOPERABIL SAU METASTATIC POZITIV LA MUTATIA BRAF V600 Data de depunere dosar 11.08.2014 Numar dosar 3035 PUNCTAJ: 65 1. DATE
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE
 RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE MINOCYCLINUM INDICAȚIA: Acnee (determinată de Propionibacterium acnes) Data de depunere dosar 08.09.2014 Numar dosar 3281 PUNCTAJ: 40 1. DATE GENERALE 1.1. DCI:
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE MINOCYCLINUM INDICAȚIA: Acnee (determinată de Propionibacterium acnes) Data de depunere dosar 08.09.2014 Numar dosar 3281 PUNCTAJ: 40 1. DATE GENERALE 1.1. DCI:
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE
 RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE EPLERENONUM INDICAȚIA: INSUFICIENŢA CARDIACĂ Data de depunere dosar 20.08.2014 Numar dosar 3160 PUNCTAJ: 55 1. DATE GENERALE 1.1. DCI: Eplerenonum 1.2.1. DC:
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE EPLERENONUM INDICAȚIA: INSUFICIENŢA CARDIACĂ Data de depunere dosar 20.08.2014 Numar dosar 3160 PUNCTAJ: 55 1. DATE GENERALE 1.1. DCI: Eplerenonum 1.2.1. DC:
Cod formular specific: L012C FORMULAR PENTRU VERIFICAREA RESPECTĂRII CRITERIILOR DE ELIGIBILITATE AFERENTE PROTOCOLULUI TERAPEUTIC DCI BORTEZOMIBUM SE
 Cod formular specific: L012C FORMULAR PENTRU VERIFICAREA RESPECTĂRII CRITERIILOR DE ELIGIBILITATE AFERENTE PROTOCOLULUI TERAPEUTIC DCI BORTEZOMIBUM SECŢIUNEA I - DATE GENERALE 1.Unitatea medicală:....
Cod formular specific: L012C FORMULAR PENTRU VERIFICAREA RESPECTĂRII CRITERIILOR DE ELIGIBILITATE AFERENTE PROTOCOLULUI TERAPEUTIC DCI BORTEZOMIBUM SECŢIUNEA I - DATE GENERALE 1.Unitatea medicală:....
MINISTERUL SĂNĂTĂȚII AGENȚIA NAȚIONALĂ A MEDICAMENTULUI ȘI A DISPOZITIVELOR MEDICALE Departamentul de Evaluare a Tehnologiilor Medicale Str. Aviator S
 RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI VEMURAFENIBUM INDICAȚIA: MELONOM MALIGN Data de depunere dosar 04.08.2014 Numar dosar 2906 PUNCTAJ: 70 1. DATE GENERALE 1.1. DCI: vemurafenib 1.2. DC: Zelboraf
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI VEMURAFENIBUM INDICAȚIA: MELONOM MALIGN Data de depunere dosar 04.08.2014 Numar dosar 2906 PUNCTAJ: 70 1. DATE GENERALE 1.1. DCI: vemurafenib 1.2. DC: Zelboraf
MINISTERUL SĂNĂTĂŢII ORDIN privind modificarea şi completarea Ordinului ministrului sănătăţii nr. 861/2014 pentru aprobarea criteriilor şi metodologie
 MINISTERUL SĂNĂTĂŢII ORDIN privind modificarea şi completarea Ordinului ministrului sănătăţii nr. 861/2014 pentru aprobarea criteriilor şi metodologiei de evaluare a tehnologiilor medicale, a documentaţiei
MINISTERUL SĂNĂTĂŢII ORDIN privind modificarea şi completarea Ordinului ministrului sănătăţii nr. 861/2014 pentru aprobarea criteriilor şi metodologiei de evaluare a tehnologiilor medicale, a documentaţiei
Strategia IT&C a Agenţiei Naţională a Medicamentului şi Dispozitivelor Medicale
 RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: LENALIDOMIDUM INDICAȚIE: LENALIDOMIDĂ SANDOZ ESTE INDICAT, ÎN ASOCIERE CU DEXAMETAZONĂ, PENTRU TRATAMENTUL PACIENŢILOR ADULŢI CU MIELOM MULTIPLU CĂRORA
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: LENALIDOMIDUM INDICAȚIE: LENALIDOMIDĂ SANDOZ ESTE INDICAT, ÎN ASOCIERE CU DEXAMETAZONĂ, PENTRU TRATAMENTUL PACIENŢILOR ADULŢI CU MIELOM MULTIPLU CĂRORA
MINISTERUL SĂNĂTĂȚII AGENȚIA NAȚIONALĂ A MEDICAMENTULUI ȘI A DISPOZITIVELOR MEDICALE Departamentul de Evaluare a Tehnologiilor Medicale Str. Aviator S
 RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE I: ACIDUM IBANDRONICUM INDICAȚIA: TRATAMENTUL OSTEOPOROZEI LA PACIENTELE ÎN POSTMENOPAUZĂ CU RISC CRESCUT DE FRACTURĂ Reducerea riscului fracturilor vertebrale
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE I: ACIDUM IBANDRONICUM INDICAȚIA: TRATAMENTUL OSTEOPOROZEI LA PACIENTELE ÎN POSTMENOPAUZĂ CU RISC CRESCUT DE FRACTURĂ Reducerea riscului fracturilor vertebrale
Strategia IT&C a Agenţiei Naţională a Medicamentului şi Dispozitivelor Medicale
 RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: INSULINUM DEGLUDEC INDICAŢIA: TRATAMENTUL DIABETULUI ZAHARAT LA ADULȚI Data depunerii dosarului 29.05.2019 Număr dosar 23402 PUNCTAJ: 85 1. DATE GENERALE
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: INSULINUM DEGLUDEC INDICAŢIA: TRATAMENTUL DIABETULUI ZAHARAT LA ADULȚI Data depunerii dosarului 29.05.2019 Număr dosar 23402 PUNCTAJ: 85 1. DATE GENERALE
CEL DE AL 4-LEA RAPORT AL COMISIEI EUROPENE PRIVIND STAREA UNIUNII ENERGETICE Conform Comunicatului Comisiei Europene din data de 9 aprilie 2019, Comi
 CEL DE AL 4-LEA RAPORT AL COMISIEI EUROPENE PRIVIND STAREA UNIUNII ENERGETICE Conform Comunicatului Comisiei Europene din data de 9 aprilie 2019, Comisia Europeană și-a îndeplinit pe deplin angajamentele
CEL DE AL 4-LEA RAPORT AL COMISIEI EUROPENE PRIVIND STAREA UNIUNII ENERGETICE Conform Comunicatului Comisiei Europene din data de 9 aprilie 2019, Comisia Europeană și-a îndeplinit pe deplin angajamentele
Strategia IT&C a Agenţiei Naţională a Medicamentului şi Dispozitivelor Medicale
 RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: PEMBROLIZUMABUM INDICAȚIA: În asociere cu pemetrexed şi chimioterapie pe bază de săruri de platină pentru tratamentul de prima linie al NSCLC metastatic
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: PEMBROLIZUMABUM INDICAȚIA: În asociere cu pemetrexed şi chimioterapie pe bază de săruri de platină pentru tratamentul de prima linie al NSCLC metastatic
Enurace Annexes I-II-III
 ANEXA I NUME, FORMA FARMACEUTICĂ, DOZAJUL PRODUSULUI MEDICAMENTOS, SPECII ANIMALE, CĂI DE ADMINISTRARE ŞI DEŢINĂTORUL AUTORIZAŢIEI DE COMERCIALIZARE 1/7 State membre Solicitant sau deţinătorul autorizaţiei
ANEXA I NUME, FORMA FARMACEUTICĂ, DOZAJUL PRODUSULUI MEDICAMENTOS, SPECII ANIMALE, CĂI DE ADMINISTRARE ŞI DEŢINĂTORUL AUTORIZAŢIEI DE COMERCIALIZARE 1/7 State membre Solicitant sau deţinătorul autorizaţiei
Săptămâna Europeană a Vaccinării # Vaccinurile sunt benefice Prevenire Să ne protejăm împreună Protecție Vaccinare aprilie 2019 Între 1 ianuarie
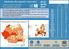 Săptămâna Europeană a Vaccinării 20-25 aprilie 2019 Între 1 ianuarie 2018 și 31 decembrie 2018, 30 de State Membre UE/SEE au raportat 12352 cazuri de rujeolă, din care 8596 (70%) au fost confirmate cu
Săptămâna Europeană a Vaccinării 20-25 aprilie 2019 Între 1 ianuarie 2018 și 31 decembrie 2018, 30 de State Membre UE/SEE au raportat 12352 cazuri de rujeolă, din care 8596 (70%) au fost confirmate cu
ÎMPREUNĂ PENTRU PACIENTUL CU SCA ÎN PRIMUL AN POST EVENIMENTUL ACUT Medicamentul BRILIQUE 90mg, DCI Ticagrelor, este 100% compensat pentru pacienții c
 ÎMPREUNĂ PENTRU PACIENTUL CU SCA ÎN PRIMUL AN POST EVENIMENTUL ACUT Medicamentul BRILIQUE 90mg, DCI Ticagrelor, este 100% compensat pentru pacienții cu SCA tratați invaziv cu stent, în baza unui contract
ÎMPREUNĂ PENTRU PACIENTUL CU SCA ÎN PRIMUL AN POST EVENIMENTUL ACUT Medicamentul BRILIQUE 90mg, DCI Ticagrelor, este 100% compensat pentru pacienții cu SCA tratați invaziv cu stent, în baza unui contract
Furosemide Vitabalans Annex I_II_ro
 Anexa I Lista numelor, formelor farmaceutice, concentraţiilor medicamentului, calea de administrare, aplicantul în Statele Membre 1 Statele Membre UE/AEE Solicitantul Denumire comercială Concentraţia Forma
Anexa I Lista numelor, formelor farmaceutice, concentraţiilor medicamentului, calea de administrare, aplicantul în Statele Membre 1 Statele Membre UE/AEE Solicitantul Denumire comercială Concentraţia Forma
COMUNICAT DE PRESĂ Agenţia Naţională a Medicamentului şi a Dispozitivelor Medicale prezintă în cele ce urmează traducerea în limba română a comunicatu
 COMUNICAT DE PRESĂ Agenţia Naţională a Medicamentului şi a Dispozitivelor Medicale prezintă în cele ce urmează traducerea în limba română a comunicatului de presă al Agenţiei Europene a Medicamentului
COMUNICAT DE PRESĂ Agenţia Naţională a Medicamentului şi a Dispozitivelor Medicale prezintă în cele ce urmează traducerea în limba română a comunicatului de presă al Agenţiei Europene a Medicamentului
Vokanamet, INN-canagliflozin-metformin
 ANEXA IV Concluzii științifice 1 Concluzii științifice Inhibitorii co-transportorului 2 de sodiu-glucoză (SGLT2) se utilizează în asociere cu regim alimentar și exercițiu fizic la pacienții cu diabet de
ANEXA IV Concluzii științifice 1 Concluzii științifice Inhibitorii co-transportorului 2 de sodiu-glucoză (SGLT2) se utilizează în asociere cu regim alimentar și exercițiu fizic la pacienții cu diabet de
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 5000/2012/ Anexa 1 Prospect Prospect: informaţii pentru pacient Aprokam 50 mg, pulbere pentru soluţie injec
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 5000/2012/01-02-03 Anexa 1 Prospect Prospect: informaţii pentru pacient Aprokam 50 mg, pulbere pentru soluţie injectabilă Cefuroximă Citiţi cu atenţie şi în întregime
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 5000/2012/01-02-03 Anexa 1 Prospect Prospect: informaţii pentru pacient Aprokam 50 mg, pulbere pentru soluţie injectabilă Cefuroximă Citiţi cu atenţie şi în întregime
COMUNICAT DE PRESĂ
 COMUNICAT DE PRESĂ Agenţia Naţională a Medicamentului şi a Dispozitivelor Medicale prezintă în cele ce urmează traducerea în limba română a comunicatului de presă al Agenţiei Europene a Medicamentului
COMUNICAT DE PRESĂ Agenţia Naţională a Medicamentului şi a Dispozitivelor Medicale prezintă în cele ce urmează traducerea în limba română a comunicatului de presă al Agenţiei Europene a Medicamentului
Furosemide Vitabalans Annex I_II_ro
 Anexa II Concluzii ştiinţifice şi motive pentru refuz prezentate de Agenţia Europeană pentru Medicamente 4 Concluzii ştiinţifice Rezumat general al evaluării ştiinţifice pentru Furosemide Vitabalans şi
Anexa II Concluzii ştiinţifice şi motive pentru refuz prezentate de Agenţia Europeană pentru Medicamente 4 Concluzii ştiinţifice Rezumat general al evaluării ştiinţifice pentru Furosemide Vitabalans şi
Strategia IT&C a Agenţiei Naţională a Medicamentului şi Dispozitivelor Medicale
 RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: DOLUTEGRAVIRUM INDICAȚIE: ÎN ASOCIERE CU ALTE MEDICAMENTE ANTIRETROVIRALE DESTINATE TRATAMENTULUI INFECŢIEI CU VIRUSUL IMUNODEFICIENŢEI UMANE (HUMAN IMMUNODEFICIENCY
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: DOLUTEGRAVIRUM INDICAȚIE: ÎN ASOCIERE CU ALTE MEDICAMENTE ANTIRETROVIRALE DESTINATE TRATAMENTULUI INFECŢIEI CU VIRUSUL IMUNODEFICIENŢEI UMANE (HUMAN IMMUNODEFICIENCY
RAPORT
 RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: Cerliponasum alfa INDICAȚIA: LIPOFUSCINOZA CEROIDĂ TIP2 (DEFICIT DE TRIPEPTIDIL PEPTIDAZA- TPP1) Data depunerii dosarului 12.12.2018 Numărul dosarului 30478
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: Cerliponasum alfa INDICAȚIA: LIPOFUSCINOZA CEROIDĂ TIP2 (DEFICIT DE TRIPEPTIDIL PEPTIDAZA- TPP1) Data depunerii dosarului 12.12.2018 Numărul dosarului 30478
Codul EFPIA privind prezentarea de informații Informări 2017 Shire Pharmaceuticals (inclusiv Baxalta US Inc.) 1
 Codul EFPIA privind prezentarea de informații Informări 2017 Shire Pharmaceuticals (inclusiv Baxalta US Inc.) 1 Secțiunea 1: Abordarea privind raportarea datelor din 2017 Pe 3 iunie 2016, Shire a achiziționat
Codul EFPIA privind prezentarea de informații Informări 2017 Shire Pharmaceuticals (inclusiv Baxalta US Inc.) 1 Secțiunea 1: Abordarea privind raportarea datelor din 2017 Pe 3 iunie 2016, Shire a achiziționat
RAPORT
 RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: RITUXIMABUM INDICAȚIE: GRANULOMATOZĂ CU POLIANGEITĂ ȘI POLIANGEITĂ MICROSCOPICA. MABTHERA, ADIMINISTRAT IN ASOCIERE CU GLUCOCORTICOIZI, ESTE INDICATĂ PENTRU
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: RITUXIMABUM INDICAȚIE: GRANULOMATOZĂ CU POLIANGEITĂ ȘI POLIANGEITĂ MICROSCOPICA. MABTHERA, ADIMINISTRAT IN ASOCIERE CU GLUCOCORTICOIZI, ESTE INDICATĂ PENTRU
Strategia IT&C a Agenţiei Naţională a Medicamentului şi Dispozitivelor Medicale
 RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: NIVOLUMABUM INDICAȚIA: In monoterapie este indicat pentru tratamentul adjuvant al melanomului extins la ganglionii limfatici sau metastazat, la adulții
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: NIVOLUMABUM INDICAȚIA: In monoterapie este indicat pentru tratamentul adjuvant al melanomului extins la ganglionii limfatici sau metastazat, la adulții
HOTĂRÂRE
 Hotărâre 18 2017-01-12 Guvernul României pentru modificarea şi completarea Hotărârii Guvernului nr. 720/2008 pentru aprobarea Listei cuprinzând denumirile comune internaţionale corespunzătoare medicamentelor
Hotărâre 18 2017-01-12 Guvernul României pentru modificarea şi completarea Hotărârii Guvernului nr. 720/2008 pentru aprobarea Listei cuprinzând denumirile comune internaţionale corespunzătoare medicamentelor
Anexa I Lista denumirilor, formelor farmaceutice, concentraţiilor medicamentelor, calea de administrare, deţinătorii autorizaţiei de punere pe piaţă d
 Anexa I Lista denumirilor, formelor farmaceutice, concentraţiilor medicamentelor, calea de administrare, deţinătorii autorizaţiei de punere pe piaţă din statele membre 1 Stat membru EU/EEA Deţinătorul
Anexa I Lista denumirilor, formelor farmaceutice, concentraţiilor medicamentelor, calea de administrare, deţinătorii autorizaţiei de punere pe piaţă din statele membre 1 Stat membru EU/EEA Deţinătorul
Vademecum in cancerul mamar incipient - Jayant S Vaidya, Vivek Patkar
 Cuprins 1. Etiopatofiziologia și riscul 7 Definiții 7 Incidența și mortalitatea 7 Structura sânului și a țesuturilor adiacente 7 Fiziopatologia 8 Factorii de risc 9 Înțelegerea riscului 13 2. Diagnostic
Cuprins 1. Etiopatofiziologia și riscul 7 Definiții 7 Incidența și mortalitatea 7 Structura sânului și a țesuturilor adiacente 7 Fiziopatologia 8 Factorii de risc 9 Înțelegerea riscului 13 2. Diagnostic
Strategia IT&C a Agenţiei Naţională a Medicamentului şi Dispozitivelor Medicale
 RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: CERITINIBUM INDICAŢIA: ÎN MONOTERAPIE ESTE INDICAT PENTRU TRATAMENTUL PACIENȚILOR ADULȚI CU CANCER PULMONAR CU CELULE NON-MICI, ÎN STADIU AVANSAT (NSCLC),
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: CERITINIBUM INDICAŢIA: ÎN MONOTERAPIE ESTE INDICAT PENTRU TRATAMENTUL PACIENȚILOR ADULȚI CU CANCER PULMONAR CU CELULE NON-MICI, ÎN STADIU AVANSAT (NSCLC),
COMISIA EUROPEANĂ Bruxelles, COM(2019) 157 final RAPORT AL COMISIEI CĂTRE CONSILIU privind progresele înregistrate de statele membre în ceea
 COMISIA EUROPEANĂ Bruxelles, 28.3.2019 COM(2019) 157 final RAPORT AL COMISIEI CĂTRE CONSILIU privind progresele înregistrate de statele membre în ceea ce privește aderarea la Convenția internațională a
COMISIA EUROPEANĂ Bruxelles, 28.3.2019 COM(2019) 157 final RAPORT AL COMISIEI CĂTRE CONSILIU privind progresele înregistrate de statele membre în ceea ce privește aderarea la Convenția internațională a
Casa Naţională de Asigurări de Sănătate MEDIC ŞEF/SERVICIUL MEDICAL Calea Călăraşilor nr. 248, Bloc S19, Sector 3, Bucureşti secretariat.medic
 Casa Naţională de Asigurări de Sănătate MEDIC ŞEF/SERVICIUL MEDICAL Calea Călăraşilor nr. 248, Bloc S19, Sector 3, Bucureşti E-mail: secretariat.medicsef@casan.ro Tel. 0372309233, Fax 0372309248 SE APROBĂ
Casa Naţională de Asigurări de Sănătate MEDIC ŞEF/SERVICIUL MEDICAL Calea Călăraşilor nr. 248, Bloc S19, Sector 3, Bucureşti E-mail: secretariat.medicsef@casan.ro Tel. 0372309233, Fax 0372309248 SE APROBĂ
Febra Periodică Asociată cu Stomatită Aftoasă, Faringită şi Adenită (PFAPA) Versiunea CE
 https://www.printo.it/pediatric-rheumatology/ro/intro Febra Periodică Asociată cu Stomatită Aftoasă, Faringită şi Adenită (PFAPA) Versiunea 2016 1. CE ESTE PFAPA 1.1 Ce este această boală? Acronimul PFAPA
https://www.printo.it/pediatric-rheumatology/ro/intro Febra Periodică Asociată cu Stomatită Aftoasă, Faringită şi Adenită (PFAPA) Versiunea 2016 1. CE ESTE PFAPA 1.1 Ce este această boală? Acronimul PFAPA
Microsoft Word - procedura mobilitati.doc
 Investeşte în oameni! FONDUL SOCIAL EUROPEAN Programul Operaţional Sectorial pentru Dezvoltarea Resurselor Umane 2007 2013 Axa prioritară nr.1 Educaţia şi formarea profesională în sprijinul creşterii economice
Investeşte în oameni! FONDUL SOCIAL EUROPEAN Programul Operaţional Sectorial pentru Dezvoltarea Resurselor Umane 2007 2013 Axa prioritară nr.1 Educaţia şi formarea profesională în sprijinul creşterii economice
Microsoft Word - EMEA ENRO
 ANEXA I LISTA CU DENUMIRILE COMERCIALE, FORMA FARMACEUTICĂ, CONCENTRAŢIA (CONCENTRAŢIILE) PRODUSULUI MEDICAMENTOS, CALEA DE ADMINISTRARE, SOLICITANTUL, TITULARUL AUTORIZAŢIEI DE INTRODUCERE PE PIAŢĂ ÎN
ANEXA I LISTA CU DENUMIRILE COMERCIALE, FORMA FARMACEUTICĂ, CONCENTRAŢIA (CONCENTRAŢIILE) PRODUSULUI MEDICAMENTOS, CALEA DE ADMINISTRARE, SOLICITANTUL, TITULARUL AUTORIZAŢIEI DE INTRODUCERE PE PIAŢĂ ÎN
Cuprins Abrevieri XIII Cuvânt-înainte XV Capitolul I. Sistemul achiziţiilor publice: concepte definitorii, evoluţie, instituţii implicate, căi de atac
 Abrevieri XIII Cuvânt-înainte XV Capitolul I. Sistemul achiziţiilor publice: concepte definitorii, evoluţie, instituţii implicate, căi de atac 1 1. Aspecte preliminare 1 2. Sediul normativ al materiei
Abrevieri XIII Cuvânt-înainte XV Capitolul I. Sistemul achiziţiilor publice: concepte definitorii, evoluţie, instituţii implicate, căi de atac 1 1. Aspecte preliminare 1 2. Sediul normativ al materiei
PowerPoint Presentation
 Săptămâna Europeană de Luptă împotriva Cancerului INFORMARE MINISTERUL SĂNĂTĂŢII INSTITUTUL NAȚIONAL DE SĂNĂTATE PUBLICĂ CENTRUL NAŢIONAL DE EVALUARE ȘI PROMOVARE A STĂRII DE SĂNĂTATE CENTRUL REGIONAL
Săptămâna Europeană de Luptă împotriva Cancerului INFORMARE MINISTERUL SĂNĂTĂŢII INSTITUTUL NAȚIONAL DE SĂNĂTATE PUBLICĂ CENTRUL NAŢIONAL DE EVALUARE ȘI PROMOVARE A STĂRII DE SĂNĂTATE CENTRUL REGIONAL
REȚELELE EUROPENE DE REFERINȚĂ AJUTORAREA PACIENȚILOR CARE SUFERĂ DE BOLI RARE SAU COMPLEXE Share. Care. Cure. Sănătate
 REȚELELE EUROPENE DE REFERINȚĂ AJUTORAREA PACIENȚILOR CARE SUFERĂ DE BOLI RARE SAU COMPLEXE Share. Care. Cure. Sănătate CE SUNT REȚELELE EUROPENE DE REFERINȚĂ? Rețelele europene de referință (ERN) [European
REȚELELE EUROPENE DE REFERINȚĂ AJUTORAREA PACIENȚILOR CARE SUFERĂ DE BOLI RARE SAU COMPLEXE Share. Care. Cure. Sănătate CE SUNT REȚELELE EUROPENE DE REFERINȚĂ? Rețelele europene de referință (ERN) [European
AUTORIZATIE DE PUNERE PE PIATĂ NR
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 2065/2009/01 Anexa 1` Prospect Aciclovir Laropharm 200 mg, comprimate Aciclovir Citiţi cu atenţie şi în întregime acest prospect înainte de a începe să utilizaţi acest
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 2065/2009/01 Anexa 1` Prospect Aciclovir Laropharm 200 mg, comprimate Aciclovir Citiţi cu atenţie şi în întregime acest prospect înainte de a începe să utilizaţi acest
Consiliul Uniunii Europene Bruxelles, 8 noiembrie 2016 (OR. en) 13583/16 BUDGET 29 EXPUNERE DE MOTIVE Subiect: Proiect de buget rectificativ nr. 4 la
 Consiliul Uniunii Europene Bruxelles, 8 noiembrie 2016 (OR. en) 13583/16 BUDGET 29 EXPUNERE DE MOTIVE Subiect: Proiect de buget rectificativ nr. 4 la bugetul general pentru exercițiul financiar 2016: Actualizarea
Consiliul Uniunii Europene Bruxelles, 8 noiembrie 2016 (OR. en) 13583/16 BUDGET 29 EXPUNERE DE MOTIVE Subiect: Proiect de buget rectificativ nr. 4 la bugetul general pentru exercițiul financiar 2016: Actualizarea
Microsoft Word - societatea informationala.doc
 I Principalii indicatori ai societăţii informaţionale la nivel naţional Indicator 2013 2014 Număr de linii telefonice fixe la 1000 de locuitori 218,4 212,6 Număr de abonaţi la telefonie mobilă la 1000
I Principalii indicatori ai societăţii informaţionale la nivel naţional Indicator 2013 2014 Număr de linii telefonice fixe la 1000 de locuitori 218,4 212,6 Număr de abonaţi la telefonie mobilă la 1000
Codul EFPIA privind prezentarea de informații Informări 2018 Shire Pharmaceuticals 1
 Codul EFPIA privind prezentarea de informații Informări 2018 Shire Pharmaceuticals 1 Secțiunea 1: Abordarea privind raportarea datelor din 2018 Pe 3 iunie 2016, Shire a achiziționat Baxalta. În conformitate
Codul EFPIA privind prezentarea de informații Informări 2018 Shire Pharmaceuticals 1 Secțiunea 1: Abordarea privind raportarea datelor din 2018 Pe 3 iunie 2016, Shire a achiziționat Baxalta. În conformitate
Microsoft Word - ORDIN pmod si comp anexei 1 la o privind aprobarea formularelor specifice pentru verificarea criteriilor
 ORDIN nr. 271 din 4 aprilie 2017 pentru modificarea şi completarea anexei nr. 1 la Ordinul preşedintelui Casei Naţionale de Asigurări de Sănătate nr. 141/2017 privind aprobarea formularelor specifice pentru
ORDIN nr. 271 din 4 aprilie 2017 pentru modificarea şi completarea anexei nr. 1 la Ordinul preşedintelui Casei Naţionale de Asigurări de Sănătate nr. 141/2017 privind aprobarea formularelor specifice pentru
Slide 1
 CENTRUL REGIONAL DE SĂNĂTATE PUBLICĂ IAŞI INSTITUTUL NAŢIONAL DE SĂNĂTATE PUBLICĂ DORINȚĂ: LIDERI PENTRU O LUME FĂRĂ TUBERCULOZĂ! PUTEȚI FACE ISTORIE. OPRIȚI TUBERCULOZA! ZIUA MONDIALĂ ÎMPOTRIVA TUBERCULOZEI
CENTRUL REGIONAL DE SĂNĂTATE PUBLICĂ IAŞI INSTITUTUL NAŢIONAL DE SĂNĂTATE PUBLICĂ DORINȚĂ: LIDERI PENTRU O LUME FĂRĂ TUBERCULOZĂ! PUTEȚI FACE ISTORIE. OPRIȚI TUBERCULOZA! ZIUA MONDIALĂ ÎMPOTRIVA TUBERCULOZEI
Deficitul de Mevalonat Kinază (DMK) (sau sindromul hiper IgD) Versiunea CE ESTE DMK 1.1
 https://www.printo.it/pediatric-rheumatology/ro/intro Deficitul de Mevalonat Kinază (DMK) (sau sindromul hiper IgD) Versiunea 2016 1. CE ESTE DMK 1.1 Ce este această boală? Deficitul de mevalonat kinază
https://www.printo.it/pediatric-rheumatology/ro/intro Deficitul de Mevalonat Kinază (DMK) (sau sindromul hiper IgD) Versiunea 2016 1. CE ESTE DMK 1.1 Ce este această boală? Deficitul de mevalonat kinază
Strategia IT&C a Agenţiei Naţională a Medicamentului şi Dispozitivelor Medicale
 RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: DOLUTEGRAVIRUM INDICAȚIA: ÎN ASOCIERE CU ALTE MEDICAMENTE ANTIRETROVIRALE DESTINATE TRATAMENTULUI INFECŢIEI CU VIRUSUL IMUNODEFICIENŢEI UMANE (HUMAN IMMUNODEFICIENCY
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: DOLUTEGRAVIRUM INDICAȚIA: ÎN ASOCIERE CU ALTE MEDICAMENTE ANTIRETROVIRALE DESTINATE TRATAMENTULUI INFECŢIEI CU VIRUSUL IMUNODEFICIENŢEI UMANE (HUMAN IMMUNODEFICIENCY
MINISTERUL SĂNĂTĂŢII APROB, Ministru Sorina PINTEA CASA NAŢIONALĂ DE ASIGURĂRI DE SĂNĂTATE APROB, p. Președinte Razvan Teohari VULCANESCU Vicepresedin
 MINISTERUL SĂNĂTĂŢII APROB, Ministru Sorina PINTEA CASA NAŢIONALĂ DE ASIGURĂRI DE SĂNĂTATE APROB, p. Președinte Razvan Teohari VULCANESCU Vicepresedinte REFERAT DE APROBARE In conformitate cu prevederile
MINISTERUL SĂNĂTĂŢII APROB, Ministru Sorina PINTEA CASA NAŢIONALĂ DE ASIGURĂRI DE SĂNĂTATE APROB, p. Președinte Razvan Teohari VULCANESCU Vicepresedinte REFERAT DE APROBARE In conformitate cu prevederile
EMA ENRO
 Anexa II Concluzii ştiinţifice şi motive pentru modificarea rezumatului caracteristicilor produsului, etichetării şi prospectului prezentate de Agenţia Europeană pentru Medicamente 23 Concluzii ştiinţifice
Anexa II Concluzii ştiinţifice şi motive pentru modificarea rezumatului caracteristicilor produsului, etichetării şi prospectului prezentate de Agenţia Europeană pentru Medicamente 23 Concluzii ştiinţifice
Microsoft Word - anunt prealabil selectie 2018.doc
 INFORMAŢII PRIVIND CONCURSURILE DE SELECŢIE PENTRU MOBILITÃŢI ERASMUS+ (KA103) IN TARILE PROGRAMULUI ERASMUS+ In perioada urmãtoare va trebui sa fiti foarte atenti la continututul anunturilor privind sesiunile
INFORMAŢII PRIVIND CONCURSURILE DE SELECŢIE PENTRU MOBILITÃŢI ERASMUS+ (KA103) IN TARILE PROGRAMULUI ERASMUS+ In perioada urmãtoare va trebui sa fiti foarte atenti la continututul anunturilor privind sesiunile
Harmonised DHPC letter_BCR-ABLTKIs_HepBreactivation_19Feb2016_PRAC version
 Martie 2016 Comunicare directă către profesioniştii din domeniul sănătăţii Inhibitori de tirozin-kinază BCR-ABL (imatinib, dasatinib, nilotinib, bosutinib, ponatinib) Necesitatea de a efectua o testare
Martie 2016 Comunicare directă către profesioniştii din domeniul sănătăţii Inhibitori de tirozin-kinază BCR-ABL (imatinib, dasatinib, nilotinib, bosutinib, ponatinib) Necesitatea de a efectua o testare
EllaOne,INN-ulipristal acetate
 Anexa IV Concluzii ştiinţifice şi motive pentru modificarea condiţiilor autorizaţiilor de introducere pe piaţă 27 Concluzii ştiinţifice Rezumat general al evaluării ştiinţifice pentru medicamentele contraceptive
Anexa IV Concluzii ştiinţifice şi motive pentru modificarea condiţiilor autorizaţiilor de introducere pe piaţă 27 Concluzii ştiinţifice Rezumat general al evaluării ştiinţifice pentru medicamentele contraceptive
PowerPoint-Präsentation
 Creditarea companiilor evoluţii şi provocări Cristian Sporis, Vicepreşedinte Raiffeisen Bank Iulie 19 1 Reducere amplă a intermedierii financiare bancare în ţările membre UE 3 4 18 Soldul creditelor acordate
Creditarea companiilor evoluţii şi provocări Cristian Sporis, Vicepreşedinte Raiffeisen Bank Iulie 19 1 Reducere amplă a intermedierii financiare bancare în ţările membre UE 3 4 18 Soldul creditelor acordate
Vă rugăm să selectați limba English STUDIU DE CONFORMITATE PENTRU SUPPLY CHAIN INITIATIVE Bine ați venit pe site-ul sondajului online Dedicated
 Vă rugăm să selectați limba English STUDIU DE CONFORMITATE PENTRU SUPPLY CHAIN INITIATIVE - 2017 Bine ați venit pe site-ul sondajului online Dedicated. Metodologia bazată pe rețeaua web garantează confidențialitatea
Vă rugăm să selectați limba English STUDIU DE CONFORMITATE PENTRU SUPPLY CHAIN INITIATIVE - 2017 Bine ați venit pe site-ul sondajului online Dedicated. Metodologia bazată pe rețeaua web garantează confidențialitatea
NOTA
 NOTĂ DE FUNDAMENTARE SECŢIUNEA 1 TITLUL PROIECTULUI DE ACT NORMATIV Hotărâre de Guvern pentru modificarea și completarea Anexei la Hotărârea Guvernului nr. 720/2008 pentru aprobarea Listei cuprinzând denumirile
NOTĂ DE FUNDAMENTARE SECŢIUNEA 1 TITLUL PROIECTULUI DE ACT NORMATIV Hotărâre de Guvern pentru modificarea și completarea Anexei la Hotărârea Guvernului nr. 720/2008 pentru aprobarea Listei cuprinzând denumirile
SPITALUL CLINIC "DR.I.CANT ACUZINO" BUCURE~TI- Str.Ion Movila Nr.5-7 Sector 2, Cod Telefon: / ; Fax: / TEMATIC
 SPITALUL CLINIC "DR.I.CANT ACUZINO" BUCURE~TI- Str.Ion Movila Nr.5-7 Sector 2, Cod 73206 Telefon: 004021/ 2.10.71.00; Fax: 004021 / 2.10.64.35 TEMATICA pentru examenul de medic specialist specialitatea
SPITALUL CLINIC "DR.I.CANT ACUZINO" BUCURE~TI- Str.Ion Movila Nr.5-7 Sector 2, Cod 73206 Telefon: 004021/ 2.10.71.00; Fax: 004021 / 2.10.64.35 TEMATICA pentru examenul de medic specialist specialitatea
Arterita Takayasu Arterita Takayasu Tradusă de Georgiana Elena Stoian după Cleveland clinic, accesată pe 22 iulie 2019 Arterita Takayasu
 Tradusă de Georgiana Elena Stoian după Cleveland clinic, accesată pe 22 iulie 2019 este o formă de vasculită în care vasele mari și mijlocii sunt inflamate și deteriorate. Corticosteroizii sunt prima linie
Tradusă de Georgiana Elena Stoian după Cleveland clinic, accesată pe 22 iulie 2019 este o formă de vasculită în care vasele mari și mijlocii sunt inflamate și deteriorate. Corticosteroizii sunt prima linie
Microsoft Word - rezumat abilitare romana.docx
 UNIVERSITATEA DE MEDICINĂ ŞI FARMACIE CAROL DAVILA BUCUREŞTI ŞCOALA DOCTORALĂ DOMENIUL MEDICINĂ TEZĂ DE ABILITARE - REZUMAT - GLAUCOMUL NOI ABORDĂRI FIZIOPATOLOGICE ȘI TERAPEUTICE CANDIDAT: CONF. DR. ALINA
UNIVERSITATEA DE MEDICINĂ ŞI FARMACIE CAROL DAVILA BUCUREŞTI ŞCOALA DOCTORALĂ DOMENIUL MEDICINĂ TEZĂ DE ABILITARE - REZUMAT - GLAUCOMUL NOI ABORDĂRI FIZIOPATOLOGICE ȘI TERAPEUTICE CANDIDAT: CONF. DR. ALINA
Analiza epidemiologica a cazurilor de tuse convulsiva,
 Analiza epidemiologica a cazurilor de pneumonie cu Legionella pneumophila intrate in sistemul national de supraveghere in anul 2018 In anul 2018 au intrat in sistemul national de supraveghere 62 cazuri
Analiza epidemiologica a cazurilor de pneumonie cu Legionella pneumophila intrate in sistemul national de supraveghere in anul 2018 In anul 2018 au intrat in sistemul national de supraveghere 62 cazuri
Erbitux, INN-cetuximab
 ANEXA I REZUMATUL CARACTERISTICILOR PRODUSULUI 1 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Erbitux 5 mg/ml soluție perfuzabilă 2. COMPOZIȚIA CALITATIVĂ ȘI CANTITATIVĂ Fiecare ml soluție perfuzabilă conține
ANEXA I REZUMATUL CARACTERISTICILOR PRODUSULUI 1 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Erbitux 5 mg/ml soluție perfuzabilă 2. COMPOZIȚIA CALITATIVĂ ȘI CANTITATIVĂ Fiecare ml soluție perfuzabilă conține
Lectia de economie. Derapaje fiscal bugetare majore in
 Lectia de economie. Derapaje fiscal bugetare majore in Uniunea Europeana. 12 tari in Procedura de Deviere semnificativa. Jumatate nu indeplinesc regulile fiscalbugetare Cristian Socol, Sistemul de reguli
Lectia de economie. Derapaje fiscal bugetare majore in Uniunea Europeana. 12 tari in Procedura de Deviere semnificativa. Jumatate nu indeplinesc regulile fiscalbugetare Cristian Socol, Sistemul de reguli
AUTORIZAŢIE DE PUNERE PE PIAŢǍ NR.6227/2006/01 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COME
 AUTORIZAŢIE DE PUNERE PE PIAŢǍ NR.6227/2006/01 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A A MEDICAMENTULUI Rowatinex picături orale,
AUTORIZAŢIE DE PUNERE PE PIAŢǍ NR.6227/2006/01 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A A MEDICAMENTULUI Rowatinex picături orale,
Imbruvica, INN-ibrutinib
 ANEXA I REZUMATUL CARACTERISTICILOR PRODUSULUI 1 Acest medicament face obiectul unei monitorizări suplimentare. Acest lucru va permite identificarea rapidă de noi informații referitoare la siguranță. Profesioniștii
ANEXA I REZUMATUL CARACTERISTICILOR PRODUSULUI 1 Acest medicament face obiectul unei monitorizări suplimentare. Acest lucru va permite identificarea rapidă de noi informații referitoare la siguranță. Profesioniștii
Microsoft Word - decizia docx
 1 www.untrr.ro www.e-rovinieta.ro DECIZIE nr. 2 din 4 decembrie 2018 privind modificarea Convenţiei privind regimul de tranzit comun [2018/1988] având în vedere Convenţia din 20 mai 1987 privind regimul
1 www.untrr.ro www.e-rovinieta.ro DECIZIE nr. 2 din 4 decembrie 2018 privind modificarea Convenţiei privind regimul de tranzit comun [2018/1988] având în vedere Convenţia din 20 mai 1987 privind regimul
EUIPO NOTES-RO Mod /2016 Note privind formularul de cerere pentru o declaraţie de anulare a unei mărci a Uniunii Europene 1. Observaţii generale
 Note privind formularul de cerere pentru o declaraţie de anulare a unei mărci a Uniunii Europene 1. Observaţii generale 1.1 Utilizarea formularului Formularul se poate obţine gratuit de la EUIPO şi poate
Note privind formularul de cerere pentru o declaraţie de anulare a unei mărci a Uniunii Europene 1. Observaţii generale 1.1 Utilizarea formularului Formularul se poate obţine gratuit de la EUIPO şi poate
Activitatea filialelor străine în România Realitatea economică arată că pe măsura dezvoltării întreprinderile tind să-şi extindă activitatea în afara
 Activitatea filialelor străine în România Realitatea economică arată că pe măsura dezvoltării întreprinderile tind să-şi extindă activitatea în afara graniţelor ţării în care ele au fost înfiinţate, acest
Activitatea filialelor străine în România Realitatea economică arată că pe măsura dezvoltării întreprinderile tind să-şi extindă activitatea în afara graniţelor ţării în care ele au fost înfiinţate, acest
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE
 RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE TRAMETINIBUM INDICAȚIA: MELANOM INOPERABIL SAU METASTATIC CU MUTAȚIE BRAF V600 ÎN MONOTERAPIE SAU ÎN ASOCIERE CU DABRAFENIB Data depunerii dosarului 24.08.2016
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE TRAMETINIBUM INDICAȚIA: MELANOM INOPERABIL SAU METASTATIC CU MUTAȚIE BRAF V600 ÎN MONOTERAPIE SAU ÎN ASOCIERE CU DABRAFENIB Data depunerii dosarului 24.08.2016
Milnacipran Pierre Fabre Medicament, INN: milnacipran
 ANEXA CONCLUZII ŞTIINŢIFICE ŞI MOTIVE ALE REFUZULUI PREZENTATE DE EMEA REZUMAT GENERAL AL EVALUĂRII ŞTIINŢIFICE PENTRU MILNACIPRAN PIERRE FABRE MEDICAMENT Milnacipran Pierre Fabre Medicament conţine milnacipran,
ANEXA CONCLUZII ŞTIINŢIFICE ŞI MOTIVE ALE REFUZULUI PREZENTATE DE EMEA REZUMAT GENERAL AL EVALUĂRII ŞTIINŢIFICE PENTRU MILNACIPRAN PIERRE FABRE MEDICAMENT Milnacipran Pierre Fabre Medicament conţine milnacipran,
PowerPoint Presentation
 Tipuri de studii clinice Descriere unui fenomen de sănătate Evaluarea unei atitudini terapeutice 1 Tipuri de studii clinice Domeniile cercetării clinice: 1. Descrierea unui fenomen de sănătate 2. Punerea
Tipuri de studii clinice Descriere unui fenomen de sănătate Evaluarea unei atitudini terapeutice 1 Tipuri de studii clinice Domeniile cercetării clinice: 1. Descrierea unui fenomen de sănătate 2. Punerea
COMUNICAT DE PRESĂ PREMIERĂ Primul pacient cu cancer tratat prin radioterapie cu Management și Monitorizare Respiratorie, la Medisprof Cancer Center,
 COMUNICAT DE PRESĂ PREMIERĂ Primul pacient cu cancer tratat prin radioterapie cu Management și Monitorizare Respiratorie, la Medisprof Cancer Center, Cluj-Napoca, România In dimineata zilei de 27 iunie
COMUNICAT DE PRESĂ PREMIERĂ Primul pacient cu cancer tratat prin radioterapie cu Management și Monitorizare Respiratorie, la Medisprof Cancer Center, Cluj-Napoca, România In dimineata zilei de 27 iunie
Minuta: 31
 Minuta: 19 martie 2019 Tema: proiectul de Hotărâre a Guvernului privind modificarea şi completarea anexei la Hotărârea Guvernului nr. 720/2008 pentru aprobarea Listei cuprinzând denumirile comune internaţionale
Minuta: 19 martie 2019 Tema: proiectul de Hotărâre a Guvernului privind modificarea şi completarea anexei la Hotărârea Guvernului nr. 720/2008 pentru aprobarea Listei cuprinzând denumirile comune internaţionale
Programe Nationale Trimestrul IV 2016
 ANEXA - MACHETE DE RAPORTARE A INDICATORILOR SPECIFICI PROGRAMELOR NAŢIONALE DE SĂNĂTATE FINANŢATE DIN BUGETUL MINISTERULUI SĂNĂTĂŢII Unitatea care derulează programul*/direcţia de sănătate publică**...
ANEXA - MACHETE DE RAPORTARE A INDICATORILOR SPECIFICI PROGRAMELOR NAŢIONALE DE SĂNĂTATE FINANŢATE DIN BUGETUL MINISTERULUI SĂNĂTĂŢII Unitatea care derulează programul*/direcţia de sănătate publică**...
LEGE Nr
 LEGE Nr. 46 din 21 ianuarie 2003 Legea drepturilor pacientului EMITENT: PARLAMENTUL PUBLICATĂ ÎN: MONITORUL OFICIAL NR. 51 din 29 ianuarie 2003 Parlamentul României adoptă prezenta lege. CAP. 1 Dispoziţii
LEGE Nr. 46 din 21 ianuarie 2003 Legea drepturilor pacientului EMITENT: PARLAMENTUL PUBLICATĂ ÎN: MONITORUL OFICIAL NR. 51 din 29 ianuarie 2003 Parlamentul României adoptă prezenta lege. CAP. 1 Dispoziţii
Microsoft Word - RO_EMEA
 ANEXA I LISTA DENUMIRILOR COMERCIALE, FORMA FARMACEUTICĂ, CONCENTRAŢIA PRODUSELOR MEDICAMENTOASE, CALEA DE ADMINISTRARE, SOLICITANŢII/ TITULARUL AUTORIZAŢIEI DE INTRODUCERE PE PIAŢĂ ÎN STATELE MEMBRE 1
ANEXA I LISTA DENUMIRILOR COMERCIALE, FORMA FARMACEUTICĂ, CONCENTRAŢIA PRODUSELOR MEDICAMENTOASE, CALEA DE ADMINISTRARE, SOLICITANŢII/ TITULARUL AUTORIZAŢIEI DE INTRODUCERE PE PIAŢĂ ÎN STATELE MEMBRE 1
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE
 RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: APIXABANUM INDICAŢIA: prevenirea evenimentelor tromboembolice venoase la pacienţii adulţi care sunt supuşi unei intervenţii chirurgicale de artroplastie
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: APIXABANUM INDICAŢIA: prevenirea evenimentelor tromboembolice venoase la pacienţii adulţi care sunt supuşi unei intervenţii chirurgicale de artroplastie
Cod formular specific: A008E Anexa nr. 1 FORMULAR PENTRU VERIFICAREA RESPECTĂRII CRITERIILOR DE ELIGIBILITATE AFERENTE PROTOCOLULUI TERAPEUTIC DCI IMI
 Cod formular specific: A008E Anexa nr. 1 FORMULAR PENTRU VERIFICAREA RESPECTĂRII CRITERIILOR DE ELIGIBILITATE AFERENTE PROTOCOLULUI TERAPEUTIC DCI IMIGLUCERASUM SECŢIUNEA I - DATE GENERALE 1.Unitatea medicală:....
Cod formular specific: A008E Anexa nr. 1 FORMULAR PENTRU VERIFICAREA RESPECTĂRII CRITERIILOR DE ELIGIBILITATE AFERENTE PROTOCOLULUI TERAPEUTIC DCI IMIGLUCERASUM SECŢIUNEA I - DATE GENERALE 1.Unitatea medicală:....
New product information wording - Dec RO
 17 December 2015 EMA/PRAC/835765/2015 Pharmacovigilance Risk Assessment Committee (PRAC) Text nou în informațiile referitoare la produs Extrase din recomandările PRAC privind semnalele Adoptat la reuniunea
17 December 2015 EMA/PRAC/835765/2015 Pharmacovigilance Risk Assessment Committee (PRAC) Text nou în informațiile referitoare la produs Extrase din recomandările PRAC privind semnalele Adoptat la reuniunea
Microsoft Word - peptic ulcer desease_ro
 Rezumat complet TITLUL GHIDULUI Boala ulceroasă peptică. BIBLIOGRAFIE Sistemul de Sănătate al Universităţii Michigan. Boala ulceroasă peptică. Ann Arbor (MI): Sistemul de Sănătate, Universitatea Michigan;
Rezumat complet TITLUL GHIDULUI Boala ulceroasă peptică. BIBLIOGRAFIE Sistemul de Sănătate al Universităţii Michigan. Boala ulceroasă peptică. Ann Arbor (MI): Sistemul de Sănătate, Universitatea Michigan;
Iron IV-A _DHPC
 Octombrie 2013 Recomandări ferme cu privire la riscul de apariţie a unor reacţii grave de hipersensibilitate la medicamentele care conţin fier şi cu administrare intravenoasă Stimate profesionist din domeniul
Octombrie 2013 Recomandări ferme cu privire la riscul de apariţie a unor reacţii grave de hipersensibilitate la medicamentele care conţin fier şi cu administrare intravenoasă Stimate profesionist din domeniul
Parlamentul României - Lege nr. 46/2003 din 21 ianuarie 2003 Legea drepturilor pacientului nr. 46/2003 În vigoare de la 28 februarie 2003 Consolidarea
 Parlamentul României - Lege nr. 46/2003 din 21 ianuarie 2003 Legea drepturilor pacientului nr. 46/2003 În vigoare de la 28 februarie 2003 Consolidarea din data de 01 martie 2018 are la bază publicarea
Parlamentul României - Lege nr. 46/2003 din 21 ianuarie 2003 Legea drepturilor pacientului nr. 46/2003 În vigoare de la 28 februarie 2003 Consolidarea din data de 01 martie 2018 are la bază publicarea
MINISTERUL SĂNĂTĂȚII DIRECȚIA POLITICA MEDICAMENTULUI ȘI A DISPOZITIVELOR MEDICALE Nr / Avizat, SECRETAR DE STAT DAN OCTAVIAN ALEXANDR
 MINISTERUL SĂNĂTĂȚII DIRECȚIA POLITICA MEDICAMENTULUI ȘI A DISPOZITIVELOR MEDICALE Nr. 29288/17.05.2019 Avizat, SECRETAR DE STAT DAN OCTAVIAN ALEXANDRESCU Aprob, MINISTRU SORINA PINTEA REFERAT DE APROBARE
MINISTERUL SĂNĂTĂȚII DIRECȚIA POLITICA MEDICAMENTULUI ȘI A DISPOZITIVELOR MEDICALE Nr. 29288/17.05.2019 Avizat, SECRETAR DE STAT DAN OCTAVIAN ALEXANDRESCU Aprob, MINISTRU SORINA PINTEA REFERAT DE APROBARE
Curriculum vitae Europass
 1 Curriculum vitae Europass Informaţii personale Nume / Prenume Oltean Galafteon Adresă 35 B-dul 1 Decembrie 1918, 540003 Târgu Mureş, Romania Telefon (40-365) 809552 Mobil: (40) 722 771065 Fax (40-265)
1 Curriculum vitae Europass Informaţii personale Nume / Prenume Oltean Galafteon Adresă 35 B-dul 1 Decembrie 1918, 540003 Târgu Mureş, Romania Telefon (40-365) 809552 Mobil: (40) 722 771065 Fax (40-265)
ORDIN privind modificarea şi completarea Ordinului ministrului sănătăţii nr. 368/2017 pentru aprobarea Normelor privind modul de calcul și procedura d
 ORDIN privind modificarea şi completarea Ordinului ministrului sănătăţii nr. 368/2017 pentru aprobarea Normelor privind modul de calcul și procedura de aprobare a prețurilor maximale ale medicamentelor
ORDIN privind modificarea şi completarea Ordinului ministrului sănătăţii nr. 368/2017 pentru aprobarea Normelor privind modul de calcul și procedura de aprobare a prețurilor maximale ale medicamentelor
Stimate pacient, Pe această cale vă aducem la cunoştinţă faptul că s-a semnat contractul cost-volum-rezultat pentru tratamentul cu Harvoni (SOFOSBUVIR
 Stimate pacient, Pe această cale vă aducem la cunoştinţă faptul că s-a semnat contractul cost-volum-rezultat pentru tratamentul cu Harvoni (SOFOSBUVIR+LEDIPASVIR) al cirozei hepatice cu virus C, forma
Stimate pacient, Pe această cale vă aducem la cunoştinţă faptul că s-a semnat contractul cost-volum-rezultat pentru tratamentul cu Harvoni (SOFOSBUVIR+LEDIPASVIR) al cirozei hepatice cu virus C, forma
31999R1228 REGULAMENTUL COMISIEI (CE) nr. 1228/1999 din 28 mai 1999 privind seriile de date care trebuie furnizate pentru statistica serviciilor de as
 31999R1228 REGULAMENTUL COMISIEI (CE) nr. 1228/1999 din 28 mai 1999 privind seriile de date care trebuie furnizate pentru statistica serviciilor de COMISIA COMUNITĂŢILOR EUROPENE având în vedere Tratatul
31999R1228 REGULAMENTUL COMISIEI (CE) nr. 1228/1999 din 28 mai 1999 privind seriile de date care trebuie furnizate pentru statistica serviciilor de COMISIA COMUNITĂŢILOR EUROPENE având în vedere Tratatul
EMA ENRO
 Anexa I Lista cu denumirile comerciale, forma farmaceutică, concentraţia medicamentelor de uz veterinar, speciile de animale, calea de administrare, deţinătorul autorizaţiilor de punere pe piaţă din statele
Anexa I Lista cu denumirile comerciale, forma farmaceutică, concentraţia medicamentelor de uz veterinar, speciile de animale, calea de administrare, deţinătorul autorizaţiilor de punere pe piaţă din statele
Asociaţia Producătorilor de Materiale pentru Construcţii din România Membră a Construction Products Europe Telefon: Fax:
 Asociaţia Producătorilor de Materiale pentru Construcţii din România Membră a Construction Products Europe Telefon:+40.724.356.404 Fax:+40-21-3211236 E-mail: office@apmcr.ro Web: www.apmcr.ro Masa Rotundă
Asociaţia Producătorilor de Materiale pentru Construcţii din România Membră a Construction Products Europe Telefon:+40.724.356.404 Fax:+40-21-3211236 E-mail: office@apmcr.ro Web: www.apmcr.ro Masa Rotundă
LEGE nr. 46 din 21 ianuarie 2003 drepturilor pacientului EMITENT: PARLAMENTUL PUBLICAT ÎN: MONITORUL OFICIAL nr. 51 din 29 ianuarie 2003 Data intrarii
 LEGE nr. 46 din 21 ianuarie 2003 drepturilor pacientului EMITENT: PARLAMENTUL PUBLICAT ÎN: MONITORUL OFICIAL nr. 51 din 29 ianuarie 2003 Data intrarii in vigoare : 28 februarie 2003 Forma actualizata valabila
LEGE nr. 46 din 21 ianuarie 2003 drepturilor pacientului EMITENT: PARLAMENTUL PUBLICAT ÎN: MONITORUL OFICIAL nr. 51 din 29 ianuarie 2003 Data intrarii in vigoare : 28 februarie 2003 Forma actualizata valabila
Opdivo, INN-nivolumab
 ANEXA I REZUMATUL CARACTERISTICILOR PRODUSULUI 1 Acest medicament face obiectul unei monitorizări suplimentare. Acest lucru va permite identificarea rapidă de noi informaţii referitoare la siguranţă. Profesioniştii
ANEXA I REZUMATUL CARACTERISTICILOR PRODUSULUI 1 Acest medicament face obiectul unei monitorizări suplimentare. Acest lucru va permite identificarea rapidă de noi informaţii referitoare la siguranţă. Profesioniştii
PRO_4657_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4657/2004/01-02-03-04-05 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR LACTECON 667 g/l lichid oral Lactuloză Citiţi cu atenţie şi în întregime acest prospect
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4657/2004/01-02-03-04-05 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR LACTECON 667 g/l lichid oral Lactuloză Citiţi cu atenţie şi în întregime acest prospect
FAQs as published on the web - EN version
 13 februarie 2017 EMA/527628/2011 Rev.1 Direcția Prezentul document oferă răspunsuri la cele mai frecvente întrebări adresate Agenției Europene pentru Medicamente (EMA). Dacă nu găsiți răspunsul la întrebările
13 februarie 2017 EMA/527628/2011 Rev.1 Direcția Prezentul document oferă răspunsuri la cele mai frecvente întrebări adresate Agenției Europene pentru Medicamente (EMA). Dacă nu găsiți răspunsul la întrebările
CASA DE ASIGURARI DE SANATATE
 Aprobat Presedintele Director General Regulament de organizare si functionare al comisiilor CAS Neamt pentru bolile cronice pentru medicamentele care necesita aprobarea Comisiei CAS Comisiile se infiinteaza
Aprobat Presedintele Director General Regulament de organizare si functionare al comisiilor CAS Neamt pentru bolile cronice pentru medicamentele care necesita aprobarea Comisiei CAS Comisiile se infiinteaza
Benlysta, INN-belimumab
 ANEXA I REZUMATUL CARACTERISTICILOR PRODUSULUI 1 Acest medicament face obiectul unei monitorizări suplimentare. Acest lucru va permite identificarea rapidă de noi informaţii referitoare la siguranţă. Profesioniştii
ANEXA I REZUMATUL CARACTERISTICILOR PRODUSULUI 1 Acest medicament face obiectul unei monitorizări suplimentare. Acest lucru va permite identificarea rapidă de noi informaţii referitoare la siguranţă. Profesioniştii
Elemente de reumatologie utilizate in recuperarea medicala OSTEOPOROZA Dr Ghita Adrian Lucian Medic specialist reumatologie Definitie- este o boala sc
 Elemente de reumatologie utilizate in recuperarea medicala OSTEOPOROZA Dr Ghita Adrian Lucian Medic specialist reumatologie Definitie- este o boala scheletala caracterizata prin compromiterea rezistentei
Elemente de reumatologie utilizate in recuperarea medicala OSTEOPOROZA Dr Ghita Adrian Lucian Medic specialist reumatologie Definitie- este o boala scheletala caracterizata prin compromiterea rezistentei
COMISIA EUROPEANĂ Bruxelles, C(2018) 2526 final REGULAMENTUL DELEGAT (UE) / AL COMISIEI din de completare a Regulamentului (UE) nr
 COMISIA EUROPEANĂ Bruxelles, 30.4.2018 C(2018) 2526 final REGULAMENTUL DELEGAT (UE) / AL COMISIEI din 30.4.2018 de completare a Regulamentului (UE) nr. 1143/2014 al Parlamentului European și al Consiliului
COMISIA EUROPEANĂ Bruxelles, 30.4.2018 C(2018) 2526 final REGULAMENTUL DELEGAT (UE) / AL COMISIEI din 30.4.2018 de completare a Regulamentului (UE) nr. 1143/2014 al Parlamentului European și al Consiliului
Aceste informații de consens privind medicamentele biosimilare au fost redactate de pacienți pentru pacienți, împreună cu reprezentanți ai Agenției Eu
 Aceste informații de consens privind medicamentele biosimilare au fost redactate de pacienți pentru pacienți, împreună cu reprezentanți ai Agenției Europene pentru Medicamente, ai Comisiei Europene și
Aceste informații de consens privind medicamentele biosimilare au fost redactate de pacienți pentru pacienți, împreună cu reprezentanți ai Agenției Europene pentru Medicamente, ai Comisiei Europene și
Evolutia mortalitatii generale in Romania
 EVOLUŢIA MORTALITĂŢII GENERALE ÎN ROMÂNIA 2013 CUPRINS 1. Tranziţia şi impactul demografic...7 2. Mortalitatea generală...12 3. Mortalitatea infantilă...26 4. Speranţa de viaţă...35 5. Tendinţele evoluţiei
EVOLUŢIA MORTALITĂŢII GENERALE ÎN ROMÂNIA 2013 CUPRINS 1. Tranziţia şi impactul demografic...7 2. Mortalitatea generală...12 3. Mortalitatea infantilă...26 4. Speranţa de viaţă...35 5. Tendinţele evoluţiei
Fişa de date Imprimantă HP Sprocket 200 Imprimi imediat fotografii de 5 x 7,6 cm (2 x 3 inchi) de la smartphone. Haide să imprimăm această petrecere.
 Fişa de date Imprimantă HP Sprocket 00 Imprimi imediat fotografii de 5 x 7,6 cm ( x 3 inchi) de la smartphone. Haide să imprimăm această petrecere. Partajează prezentul cu fotografii instantanee de 5 x
Fişa de date Imprimantă HP Sprocket 00 Imprimi imediat fotografii de 5 x 7,6 cm ( x 3 inchi) de la smartphone. Haide să imprimăm această petrecere. Partajează prezentul cu fotografii instantanee de 5 x
